La C.M.H
Cardiomyopathie obstructive (CMO) et Cardiomyopathie hypertrophique (CMH), recommandations aux éleveurs
Chris Amberger, Dr Med Vet, DECVIM-CA(Cardiology)
http://esvc.ch/
D’après Kittleson, Gompf et Little: Feline Hypertrophic
Cardiomyopathy: advice for Breeders

Qu’est-ce que la cardiomyopathie hypertrophique?
Les CMO et CMH sont des maladies génétiques caractérisées
par un épaississement des parois du coeur au détriment des cavités internes.
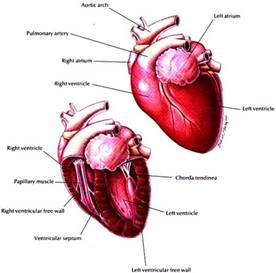
Coeur normal : l’épaisseur des parois est plus petite que la dimension interne
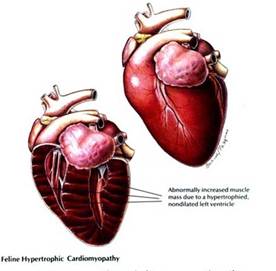
Cœur hypertrophique: les parois sont fortement épaissies au détriment des cavités internes
La cardiomyopathie hypertrophique est, chez l’homme, une des grandes responsables de la mort subite chez le jeune adulte. Le complexe CMO/CMH est la maladie cardiaque la plus courante présente chez le chat, quelle que soit la race, avec une recrudescence particulière chez le Maine Coon. Cette maladie a été observée chez des chatons de quelques mois comme chez des adultes de plus de 10 ans.
L’épaississement progressif de la musculature cardiaque se traduit d’abord par un agrandissement des muscles papillaires, puis de l’intégralité du myocarde des ventricules. Si le chat est porteur du gène responsable de cette maladie dès la naissance, il ne développera la maladie qu’en fin de croissance, vers 2 ans pour le mâle et 3 ans pour la femelle. Le développement de l’hypertrophie de la musculature est progressif, conduisant à des modifications de la fonction cardiaque, des arythmies (responsables de mort subite) et une tendance à la formation de caillots dans les atrias (responsable de thromboses aortiques).
Lors de l’apparition de symptômes cliniques causés par l’insuffisance cardiaque, il est souvent trop tard pour traiter le chat de manière efficace.
L’expression phénotypique de l’épaississement du myocarde est extrêmement variable, rendant le diagnostic de la maladie difficile dans les stades précoces.
Quelle est la cause de CMO/CMH chez le chat ?
Le rôle de l’hérédité dans la genèse de cette maladie a été mis en évidence chez le Maine Coon (Kittleson et al. Circulation, 1998), où la transmission familiale a été mis en évidence.
Il existe malheureusement plusieurs mutations de la protéine contractile des muscles cardiaques (myosine). La myosine mutée ayant une activité réduite, l’hypertrophie cardiaque est un phénomène compensatoire visant à essayer de maintenir un débit cardiaque normal.
L’hypertrophie des muscles cardiaques peut également être causée par d’autres maladies, comme l’hypertension artérielle et hyperthyroïdisme. Si la CMH/CMO est une maladie primaire, l’hypertension et l’hyperthyroïdisme causent un épaississement de la musculature cardiaque secondaire à un problème circulatoire. Le diagnostic de CMO/CMH génétique chez un chat âgé de plus de 5 ans ne devrait se faire qu’après exclusions des autres causes possibles.
Est-ce que la CMO/CMH est génétique ?
Les nombreuses mutations (plus de 200 à ce jour) de plusieurs gènes (10) sur plusieurs chromosomes différents ont été découvertes chez l’homme. Chez le chat, la transmission dominante autosomale a été confirmée, avec une expression variable, ce qui signifie que la présence d’un seul gène anormal chez un des parents est suffisante pour être transmise aux descendants. Il est également possible de trouver des porteurs génétiques qui ne développent pas la maladie. Un chaton peut donc être testé positif même si ses deux parents ont été déclarés négatifs. L’expression clinique de la maladie est très variable, certains animaux seront grièvement touchés, d’autres de manière beaucoup plus discrète, et certains ne seront pas affectés alors qu’ils pourront transmettre le gène mutant.
Le mode de transmission est le suivant : les mâles et les femelles sont affectés de manière égale, chaque animal développant la maladie l’a acquis de l’un de ses deux parents (ou des deux) et va transmettre le gène anormal à la moitié de sa descendance.
L’étude du support génétique de la maladie chez le Maine Coon (HCM1), basé sur l’observation d’une famille touchée, est le suivant :
– autosomal dominant à 100% de pénétrance, mais avec expression variable
– les homozygotes développent la maladie rapidement (environ 1 an de survie)
– les hétérozygotes ont des formes plus modérées
– pas de signes d’expression phénotypique avant l’âge de 6 mois, puis développement d’une hypertrophie des muscles papillaires, le plus souvent associée à un souffle cardiaque
– évolution vers une mort subite (arythmie) avec un décès entre 1 et 2 ans pour les homozygotes, 3 à 6 ans pour les hétérozygotes
La mutation du gêne cMyBP-C3 a été mise en évidence chez le Maine Coon, produisant une altération des sarcomères sur la chaine lourde de la myosine responsable de la désorganisation des fibres cardiaques, avec fibrose interstitielle secondaire et développement d’artériosclérose coronarienne. La mutation découverte chez le Maine Coon est probablement différente chez les autres races de chats. Des recherches génétiques sont en cours pour les autres races.
Existe-t-il une origine alimentaire à la CMO/CMH ?
Aucune cause nutritionnelle n’a été mise en évidence à ce jour chez le chat ou l’homme. De même, aucun ajout alimentaire (taurine, carnitine, vitamines, etc..) ne permet de soigner la CMO/CMH.
Comment la CMO/CMH est-elle diagnostiquée ?
La CMO/CMH est mise en évidence par un examen cardiaque aux ultrasons (échocardiographie). C’est le meilleur moyen pour détecter les anomalies de la musculature cardiaque. L’échocardiographie conventionnelle, sans arriver à la précision du Doppler Tissulaire, est une méthode efficace pour dépister la CMH/CMO de manière précoce.
Réalisation de l’examen cardiaque :
Il s’agit d’abord d’un examen clinique complet, avec auscultation et recherche d’un éventuel souffle cardiaque, de la mesure de la fréquence cardiaque au repos et du poids corporel.
L’examen échographique prend en compte :
1. L’appréciation générale de la taille des cavités, de la forme des parois, de la structure des muscles papillaires et de la densité échographique du myocarde. Estimation du rapport entre les parois droites et gauches en relation avec le septum interventriculaire.
2. La description des structures et du mouvement des 4 valves cardiaque, particulièrement de la mitrale (valve atrio-ventriculaire gauche)
3. La mesure précise de la dimension des parois en diastole, dont les valeurs moyennes statistiques pour chaque race sont connues par rapport au poids corporel.
4. Les mesures des dimensions de l’aorte, de l’atrium gauche et du tronc pulmonaire
5. L’examen au Doppler couleur en cas de souffle cardiaque afin de confirmer l’origine ou la cause de ce souffle
6. La mesure de la vitesse au Doppler dans la chambre de chasse ventriculaire gauche et droite, ainsi que la présence éventuelle d’une obstruction dynamique gauche ou droite.
7. La confirmation d’un défaut d’étanchéité des valves mitrales ou tricuspide au Doppler en cas de dilatation atriale
Le protocole de dépistage officiel établi par le Collège Américain de Cardiologie Animale (ACVIM-Cardiology) inclut principalement ces 7 paramètres et leur variation. Ce dépistage est recommandé chez tous les chats d’élevage, avec répétition annuelle pour les chats sains, tous les 6 mois pour les chats équivoques et chez tous les animaux dont un parent dans les 2 générations ascendantes ou descendantes a été touché par cette maladie.
Si l’échocardiographie effectuée par un spécialiste est un bon moyen de dépistage des formes avancées de CMO/CMH, la détection des formes minimes ou en évolution reste très difficile. Idéalement, l’examen cardiaque devrait être fait par un spécialiste en cardiologie (DACVIM ou DECVIM-CA).
Quelles sont les « valeurs normales » :
On appelle « Valeur normale » la valeur statistique comprenant la variation dans laquelle 95% de la population saine se trouve. Toute valeur supérieure (2.5%) ou inférieure (2.5%) à cette moyenne est considérée comme « Hors norme ». Les moyennes sont établies en général sur la base d’une population de 100 individus (50 mâles et 50 femelles) normaux et la valeur de référence est publiée dans des études spécifiques effectuées, actuellement disponible chez le Maine Coon (Drourr 2005), le chat Européen (Chetboul 2005) et le Sphynx (Amberger et Chetboul, 2006).
Définition du chat « Normal » selon le formulaire « officiel » de Kittleson : animal ne présentant pas de souffle cardiaque, pas d’arythmie cardiaque, dont l’examen cardiaque global à l’échographie est normal, et dont les 7 mesures effectuées sont toutes dans la norme.
Définition du chat « Equivoque » : Chat dont les mesures de la paroi ventriculaire ou du septum sont comprise dans l’intervalle de confiance (ou dans la norme), mais dont une ou plusieurs anomalies cardiaque sont décelée (souffle cardiaque, hypertrophie ou hyperéchogénicité des muscles papillaires, mouvement anormal de la valve mitrale, dilatation atriale gauche..)
Définition du chat « Suspect de CMH) : Chat ayant plus de 3 facteurs anormaux sur les 7, dont les mesures de l’épaisseur des parois sont à la limite supérieure
Définition du chat « Positif » : Chat ayant plus de 4 facteurs anormaux sur les 7, dont les mesures des parois sont toutes supérieures à la normale.
Définition du chat « Positif , forme avancée » : Chat dont tous les facteurs sont modifié, ayant développé des signes cliniques d’insuffisance cardiaque.
En règle générale, une dimension diastolique des parois supérieure à 6 mm pour un chat de 5 kg est la limite établie pour le diagnostic de l’hypertrophie du myocarde, pour autant que les autres signes typiques (anomalie des muscles papillaires, mouvement anormaux de la valve mitrale, dilatation atriale gauche) soient présents.
Le dépistage génétique chez le Maine Coon pour la mutation cMyBP-C (aussi appelée HCM1) développé par le Dr K. Meurs (http://www.vetmed.wsu.edu/deptsvcgl/) permet d’identifier les chats porteurs de la mutation. Les chats porteurs d’une copie du gène sont appelés hétérozygotes, ceux porteurs de 2 copies homozygotes. Ce test a été repris en Europe par 2 laboratoires, Antagène et Laboclean. L’intérêt majeur du dépistage génétique est qu’il peut se faire dès le plus jeune âge sur la base d’un frottis buccal ou d’un prélèvement sanguin. Son coût est sensiblement similaire à celui d’une échographie.
Une fois la maladie déclarée, d’autres examens permettent de confirmer la présence d’une hypertrophie cardiaque comme la radiographie, qui permet également d’estimer le degré de congestion pulmonaire, ou l’électrocardiogramme (présence fréquente d’arythmies cardiaques)
Chez le chat plus âgé, la mesure de la pression artérielle ainsi qu’un test sanguin de la glande thyroïde sont indiqués afin d’exclure la présence d’une hypertrophie cardiaque secondaire à une autre maladie.
Sur quoi se baser pour le diagnostic de la CMO/CMH ?
Statistiquement, certaines races sont plus exposées au risque de CMO/CMH.
Dans nos résultats sur les 10 dernières années (600 chats), 3/4 des animaux présentaient de maladies cardiaques acquises, et plus de 2/3 une CMO/CMH.
Parmi les races à risque, ou dont l’incidence est supérieure à l’Européen :
– le Maine Coon
– le Sphynx
– le Chartreux et le British Shorthair
– Le Chat des forêts Norvégiennes
– Le Burmese
– L’Américain à poil court
Les autres races ont une représentation similaire à l’Européen (Scottish fold, Persan, Sibérien, Siamois), ou sont moins sensibles à la maladie (Sacré de Birmanie, Devon rex, Abyssin, Oriental, Singapura)
Le signe clinique le plus fréquent sera l’apparition d’un souffle cardiaque lié au changement de géométrie cardiaque, apparaissant dès le commencement de l’hypertrophie des muscles papillaires, en relation ou non avec les mouvements anormaux de la valve mitrale (séparant le ventricule de l’atrium gauche).
Les tests de dépistage sanguins biochimiques (myoglobine, troponines, ANP/BNP) n’ont pas donnés les résultats escomptés à ce jour. Il ne peuvent être utiles que pour confirmer une forme avancée de la maladie, visible également sur les radiographies thoraciques et ne sont absolument pas un indicateur précoce de la mutation, spécialement les troponines cardiaques qui n’augmentent qu’en stade terminal de la maladie.
Problématique du dépistage :
L’échographie pose un problème pour plusieurs raisons. L’accès à un centre spécialisé n’est pas accessible à tous les éleveurs, et le facteur financier représente une certaine limite. Comme la CMO/CMH peut apparaître à n’importe quel âge, un examen isolé ne garanti en aucune manière que le chat ne développera pas la maladie dans le futur.
Chez le Maine Coon, un chat testé génétiquement négatif au HCM1 (mutation cMyBP-C) ne signifie pas que le chat est libre de CMO/CMH, d’autres mutations pouvant être présentes. Le test génétique permet d’éliminer de l’élevage les animaux positifs au HCM1 dès le plus jeune âge. Les animaux négatifs seront suivis échographiquement par la suite comme les autres races.
L’élevage impose 2 impératifs :
– établir un diagnostic avant l’âge de mise en reproduction
– établir un diagnostic par des moyens pratiques et économiques
A partir de quand, et à quel intervalle les chats doivent-ils être testés ?
Lorsqu’un chat présente des signes cliniques (difficulté respiratoire, souffle cardiaque, thrombose et embolie périphérique), il devrait obligatoirement être examiné rapidement afin d’essayer de traiter les signes cliniques d’insuffisance cardiaque.
Les tests des chats pour un programme d’élevage sont plus délicats. L’échocardiographie n’est pas un instrument parfait. Certains animaux avec une expression modérée de la maladie pourraient ne pas être décelés, particulièrement si le matériel utilisé ou la formation de l’examinateur ne sont pas adéquats.
Comme la CMO/CMH est une maladie se développant plus ou moins rapidement, un examen unique ne garantit pas que le chat ne développe pas d’hypertrophie 6 mois ou une année après.
Comme pour le dépistage génétique, si un test positif à l’échographie est fiable à 100%, il n’en est pas de même pour un test négatif.
Les chats d’élevage devraient probablement avoir un dépistage annuel pendant leur période de reproduction, malgré les frais élevés de ce mode d’examen.
De même, tout animal décédé de manière inexpliquée devrait être autopsié, afin de confirmer l’origine cardiaque du décès (d’autres causes sont également possibles), et ne pas condamner inutilement les parents et la descendance à cause d’un autre problème (infectieux, traumatique, autre…)
Un cœur dont le poids dépasse 20 grammes, et dont l’histologie présente des altérations de structure typiques dans le myocarde peut être classé HCM avec certitude. Malheureusement, peu de centres de pathologie sont à même d’identifier ces modifications microscopiques.
Quel est l’âge adéquat pour les tests CMO/CMH ?
Chez le Maine Coon, la majorité des mâles touchés auront des signes décelables à l’échographiques à l’âge de 2 ans et la majorité des femelles à l’âge de 3 ans.
Bien qu’il n’y ait pas de consensus actuel sur l’âge minimal, les experts du groupe suisse de cardiologie vétérinaire recommandent d’attendre l’âge de 18 mois pour faire les tests échographiques CMH
Les chatons Maine Coon peuvent être testés génétiquement dès l’âge de 3 semaines. Attention, la salive seule ne contient pas assez d’ADN, il est important de bien pratiquer un brossage cytologique complet en roulant la brosse plusieurs fois contre les gencives et en pressant la joue, de manière à ce que des cellules de tissus gingival soient prélevées. Un test pratiqué que sur la salive risque d’être négatif alors que le chat est porteur du gène.
Quels sont les endroits en Suisse où le dépistage échographique peut être effectué ?
Facultés de médecine vétérinaire :
Tierspital Zürich, Département de cardiologie
(Directeur : Dr Tony Glaus DECVIM/ACVIM) tél. 01 635 83 06
Tierspital Bern, Département de cardiologie
(Directeur : Prof. C.W. Lombard DACVIM/ECVIM) tél. 031 631 23 15
Centre référé en imagerie à Genève :
Cabinet-Vétérinaire Amberger-Philip 96 rue de la Servette 1202 Genève
(Dr Christophe Amberger DECVIM, Dr Valérie Schmid DECVDI) tél. 022 734.42.48
Comment éliminer la CMO/CMH de mon élevage ?
Les moyens dont nous disposons actuellement pour le diagnostic de la CMO/CMH (dépistage génétique, échocardiographie et autopsie) ne nous permettent pas d’éliminer toutes les formes de cardiomyopathies avec certitude. Cependant, les éleveurs pratiquant un dépistage systématique depuis plusieurs années ont vu l’incidence de CMO/CMH drastiquement réduite.
Chez le Maine Coon, l’association du dépistage génétique et de l’échographie permet d’éliminer rapidement de l’élevage les porteurs de la mutation et ceux chez qui une hypertrophie est présente.
La centralisation des données génétiques est importante. Elle permettra par la suite des analyses de pedigree, permettant de calculer le risque de maladie en fonction de l’origine des géniteurs (calcul des risques d’expression des gènes en fonction du choix des parents).
Deux parents normaux peuvent-il avoir un chaton porteur ?
Depuis que la génétique de cette maladie est connue, il est établi que tout animal positif au gène de la CMH1 doit avoir un des parents porteurs du gène. Cependant, plusieurs situations existent dans lesquelles un chaton porteur du gène ait des parents apparemment normaux.
La première possibilité est qu’un des parents soit positif mais non diagnostiqué (erreur de dépistage génétique – salive à la place de tissus des gencives-, mauvaise interprétation de l’examen échographique, mauvaise qualité de l’échographie, matériel inadéquat, etc..). Cela peut également se produire, si les examens échographiques ne sont pas répétés chaque année, la maladie se développant parfois après l’âge de 4 ans.
D’autres modifications génétiques étant présentes, il est également possible que les parents d’un chat développant une CMO/CMH précoce soient négatifs au gène HCM1 et également négatifs à l’échographie à un âge avancé, mais porteur d’un gène anormal.
Que dois-je faire si mon chat est atteint de CMO/CMH ?
Les chats dépistés positifs à la CMO/CMH devraient être retirés de l’élevage, et toute la descendance contrôlée afin d’éviter la dissémination du gène muté.
Statistiquement, 50% des portées obtenues avec un chat malade seront porteurs du gène.
Les parents d’un chat dépistés positivement devraient également être contrôlés, puisque l’un des deux (ou les deux) est porteur de la mutation.
L’incidence de mutation spontanée étant rare, les parents et grands parents d’un animal positif au HCM1 ou ayant développé une hypertrophie devraient être contrôlés, ainsi que toute sa descendance.
Traitement de la cardiomyopathie hypertrophique :
A l’heure actuelle, il n’existe aucun traitement permettant de guérir la CMH/CMO.
Si l’hypertrophie de la musculature cardiaque est le résultat d’une autre maladie, le traitement de la maladie primitive va améliorer spontanément la fonction cardiaque.
L’hypertrophie de la musculature cardiaque empêche une fonction normale du cœur. Plusieurs médicaments sont souvent nécessaires afin d’empêcher le développement d’une insuffisance cardiaque définitive.
Les options de traitement dépendent de l’état clinique de l’animal, ainsi que du type de cardiomyopathie rencontré.
Le traitement cardiaque devra à la fois améliorer le travail du cœur, réduire la charge cardiaque afin d’éviter l’apparition d’œdème et prévenir le risque d’embolie périphérique.
Si un chat présente des signes sévères d’insuffisance cardiaque ou de paralysie/parésie d’un membre, un traitement en urgence sera indispensable. Le pronostic de la maladie est alors très sombre.
Le stade du développement de cardiomyopathie hypertrophique est déterminant pour le choix du traitement. Si un animal en stade précoce ne présente aucun symptôme, une forme avancée de la maladie est généralement associée à de nombreux signes cliniques.
La qualité de vie de l’animal est le facteur le plus important en ce qui concerne la décision de traiter ou d’endormir, selon les possibilités de confort que nous pouvons lui offrir.
Les sites à visiter:
www.winfelinehealth.org/health/hypertrophic-cardiomyopathy.html
http://www.cardiomyopathie.org/
http://www.scf-fr.net/index.php?doc=include/site/doc_inc.cmh.php

Glossaire:
Arythmie : battements cardiaques irréguliers
Autosomal : Chromosome non sexuel (hors XY)
Atrium, atrias: partie supérieure du cœur,
ancienne appellation : oreillettes
Cardiomyopathie : maladie du muscle cardiaque
cMyBP-C3 : Gène codant une des protéines cardiaque
Diastole : relaxation cardiaque
Dominant : gène s’exprimant seul
Embolie périphérique : caillot de sang obstruant les artères
p.ex. thrombose aortique
Histologie : Analyse microscopique des tissus
Hyperéchogénicité : modification de la densité du myocarde
à l’échographie
Récessif : gène devant être doublé pour s’exprimer
Systole : contraction cardiaque

Ce texte a été élaboré en collaboration avec le groupe Suisse de cardiologie Vétérinaire (président, Dr. T. Glaus, DECVIM/DACVIM)



